Technologie
Une innovation de rupture dans le traitement des maladies microscopiques résiduelles
Technologie
Innovation thérapeutique
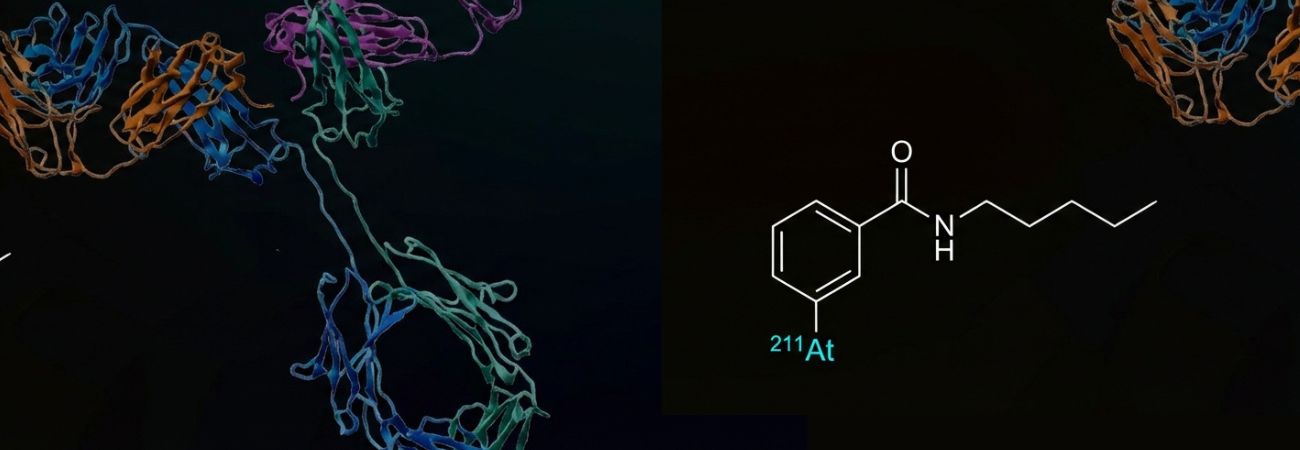
La technologie développée par Atonco est une innovation de rupture très prometteuse dans l’éradication des maladies microscopiques résiduelles ou des cellules tumorales résiduelles isolées ou groupées, rapidement accessibles à un radiopharmaceutique marqué à l’astate-211.
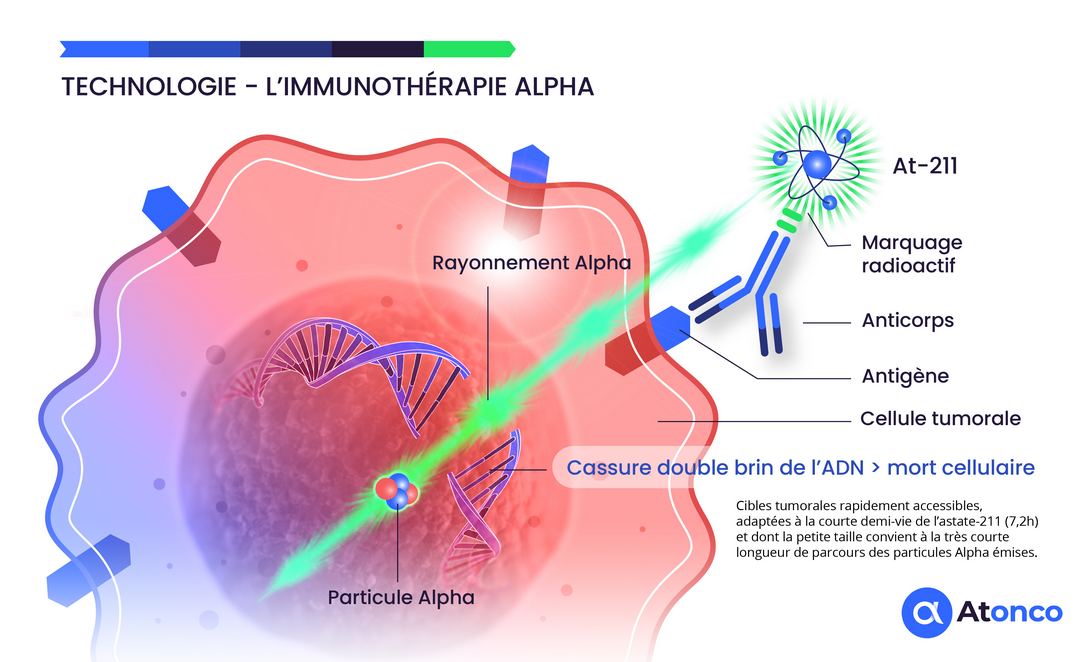
L’utilisation de radionucléides émetteurs de particules alpha est un fait d’actualité et présente un grand intérêt médical en raison de l’effet cytotoxique élevé de ces particules alpha sur les cellules tumorales qui se traduit par des cassures double brin de l’ADN. En outre, cette utilisation entraine une bonne tolérance du fait du court trajet des particules alpha épargnant potentiellement les tissus normaux proches des cibles tumorales.
Pourquoi l’Astate 211 ?
L’astate-211 (²¹¹At) représente le radionucléide émetteur alpha optimal pour la thérapie ciblée en raison de ses propriétés physiques et chimiques uniques. Sa demi-vie de 7,2 heures offre un équilibre idéal entre le temps nécessaire pour la production, la purification, la conjugaison et l’administration thérapeutique, tout en minimisant l’exposition systémique prolongée.
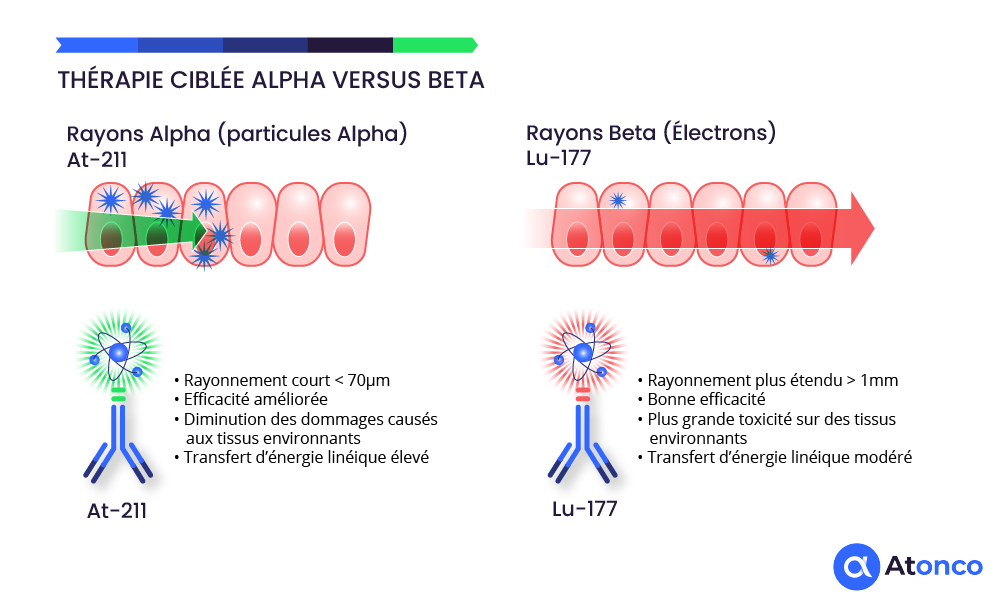
Les particules alpha émises par l’²¹¹At possèdent une énergie de 5,9 MeV avec un parcours tissulaire de 55-80 μm, correspondant à 5-10 diamètres cellulaires. Cette caractéristique permet une destruction sélective des cellules tumorales ciblées tout en préservant les tissus sains adjacents, offrant ainsi un index thérapeutique exceptionnellement favorable.
Le transfert d’énergie linéique (TEL) élevé de ~100 keV/μm induit des dommages irréparables de l’ADN, indépendamment du statut d’oxygénation des cellules tumorales. Cette propriété s’avère particulièrement avantageuse pour le traitement des tumeurs hypoxiques, souvent résistantes aux thérapies conventionnelles.
Bibliographie
Cancer de la vessie
Application clinique
Alpha-immunothérapie du cancer de vessie non infiltrant le muscle (TVNIM) avec un anticorps chimérique anti-Anhydrase Carbonique IX (CAIX), girentuximab, marqué à l’astate-211: notre candidat, l’ATO-101™
L’ATO-101™ cible le tumeurs de la vessie n’infiltrant pas le muscle, réfractaire au BCG et à la chimiothérapie et en attente d’une cystectomie totale.
L’ATO-101™, notre candidat radiopharmaceutique est un anticorps anti-CAIX marqué à l’astate-211 à l’aide d’une technologie de radiomarquage protégée, et développée à Nantes, en France.
L’antigène CAIX est exprimé sur la membrane des cellules cancéreuses des tumeurs superficielles n’infiltrant pas le muscle de la vessie et donc directement et rapidement accessibles pour l’anticorps anti-CAIX radiomarqué instillé par voie intravésicale. De plus, les récidives qui surviennent fréquemment après des traitements répétés au BCG ou à la chimiothérapie sont constituées de fines couches de cellules cancéreuses qui répondent bien à la très courte longueur de trajet des particules alpha émises. Ainsi, la situation du tumeurs de la vessie n’infiltrant pas le muscle correspond bien aux caractéristiques radiophysiques des particules alpha.

Les tumeurs ont une faible épaisseur correspondant bien à la très courte longueur de trajet (<0,1 mm) des particules alpha et leur localisation superficielle dans la cavité vésicale les rend accessibles à un radiopharmaceutique instillé par voie intravésicale. De plus, la situation clinique des patients réfractaires au traitement conventionnel utilisant la thérapie BCG ou la chimiothérapie et pour lesquels le risque d’une cystectomie totale inconfortable justifie la mise en œuvre de l’immunothérapie alpha innovante délivrée par instillation intravésicale.
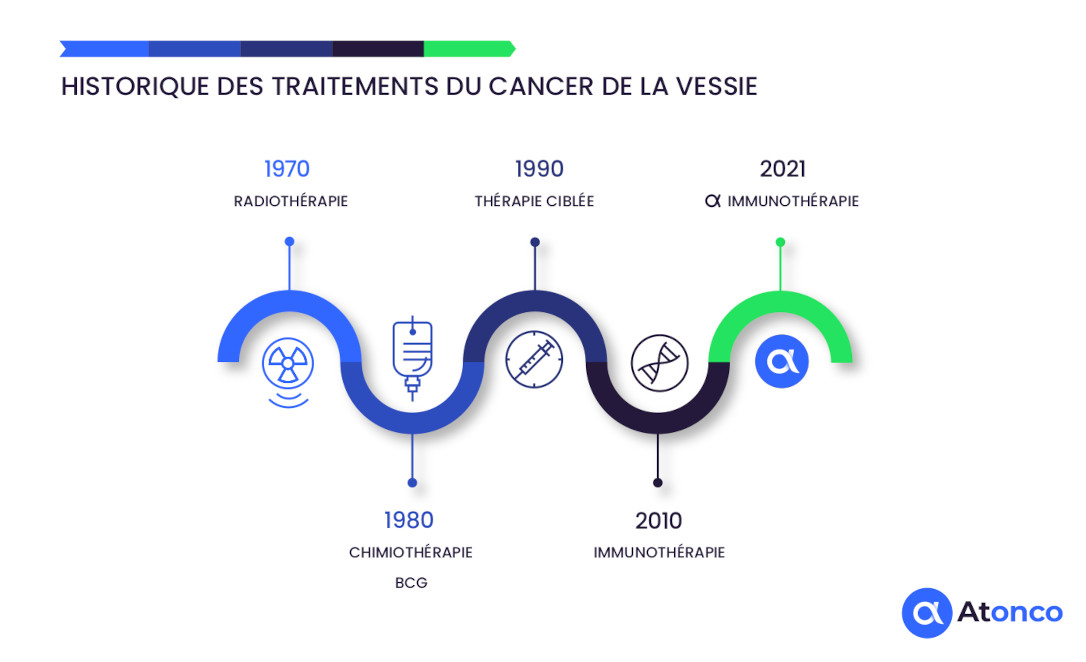
Historique des traitements du cancer de la vessie
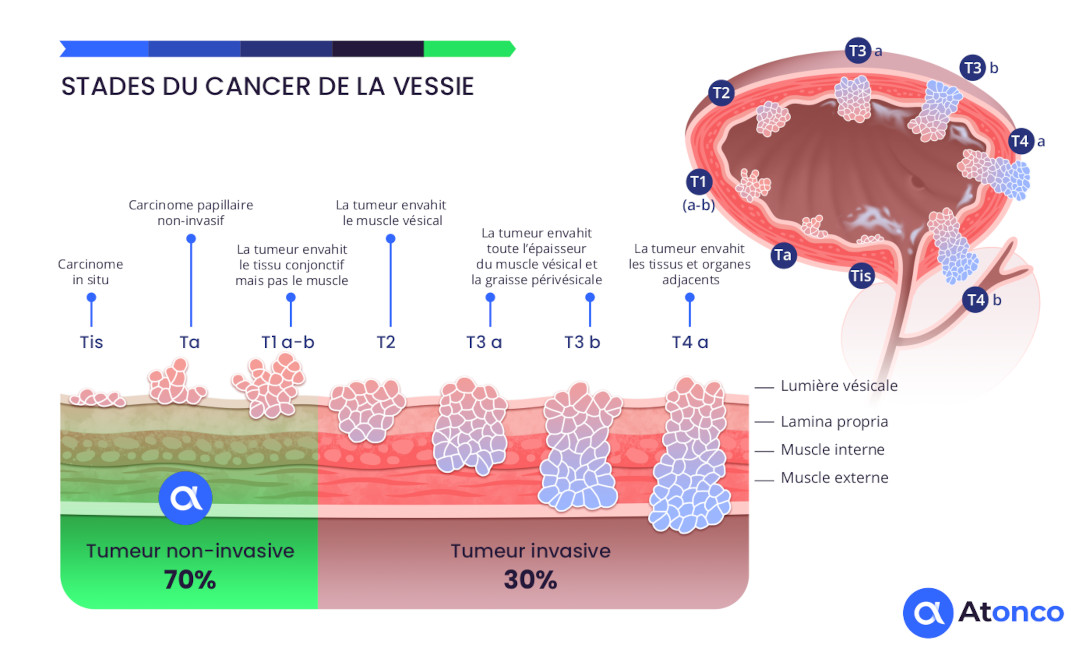
Stades du cancer de la vessie
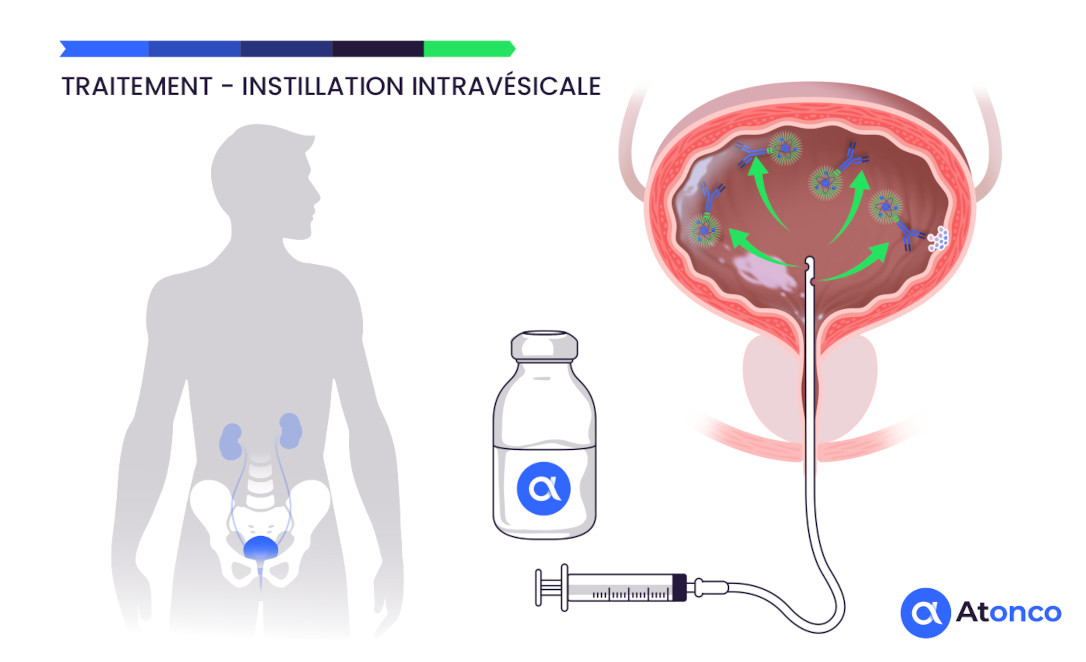
Traitement – Instillation intravésicale
Bibliographie
Thérapie alpha ciblée
Traitement innovant
La thérapie alpha ciblée utilisant l’Astate-211 représente une avancée majeure dans le traitement des maladies cancéreuses, offrant des avantages décisifs par rapport aux approches thérapeutiques conventionnelles.
Avantages des particules alpha par rapport aux traitements classiques
Les particules alpha présentent des avantages décisifs pour tuer les cellules tumorales par rapport à la radiothérapie externe et la chimiothérapie, notamment grâce à leur efficacité biologique supérieure et leur toxicité limitée aux tissus sains avoisinants. Leur très haute énergie linéique de transfert (100 fois supérieure à celle des rayonnements bêta (électrons) provoque des cassures double brin irréparables de l’ADN, ce qui conduit à une destruction irréparable des cellules cancéreuses. De plus, la portée très courte des particules alpha (quelques cellules seulement) limite les dégâts aux cellules saines proches, ce qui réduit les effets secondaires indésirables souvent observés avec la radiothérapie externe et la chimiothérapie.
Efficacité biologique et mécanisme d’action
Contrairement aux traitements comme la chimiothérapie qui nécessitent une internalisation cellulaire prolongée, l’alphathérapie ciblée peut tuer les cellules tumorales grâce aux dégâts immédiats causés par les particules alpha sur l’ADN sans nécessiter une internalisation du vecteur. Une à trois particules alpha suffisent à tuer une cellule tumorale alors que des milliers de particules bêta ou molécules de chimiothérapie sont nécessaires. Cette efficacité ciblée est particulièrement adaptée aux micro-métastases et aux petits agrégats tumoraux résiduels comme dans le cas du cancer de la vessie n’envahissant pas le muscle après résection de lésions macroscopiques.
Toxicité limitée et ciblage précis
La courte portée des particules alpha dans les tissus (2 à 5 couches cellulaires) permet une concentration très locale de la dose, réduisant ainsi la toxicité sur les tissus sains environnants, contrairement à la radiothérapie externe plus diffuse ou à la chimiothérapie qui peut affecter plusieurs types de cellules. Ce ciblage est rendu possible grâce à l’utilisation de vecteurs biologiques (anticorps, peptides) qui transportent le radioisotope alpha directement vers les cellules tumorales, ce qui diminue la zone d’exposition et les effets secondaires systémiques.
Comparaison avec la radiothérapie externe et la chimiothérapie
Radiothérapie externe : traite souvent une large zone tumorale et environnante, exposant ainsi des tissus sains à des radiations, pouvant causer des effets secondaires importants. Sa pénétration plus large est moins adaptée aux petites lésions dispersées.
Chimiothérapie : agit de manière systémique, affectant aussi des cellules saines avec des toxicités multiples, notamment hématologiques et gastro-intestinales.
Alphathérapie : cible avec précision les cellules cancéreuses, minimise les dommages collatéraux et optimise la destruction cellulaire même dans des zones difficiles d’accès comme les micro-métastases.
Ces avantages font de la thérapie par particules alpha une approche thérapeutique prometteuse et complémentaire, notamment dans les cancers résistants aux traitements classiques, en offrant un meilleur rapport efficacité : toxicité.
